L’incidence annuelle au cours de la cirrhose du carcinome hépatocellulaire (CHC), qui est la dénomination du cancer du foie, est de l’ordre de 1 à 5 %. Cela justifie de mettre en place un dépistage systématique chez tous les patients atteints de cirrhose.

Le carcinome hépatocellulaire (CHC) se développe habituellement sur une cirrhose (75 à 80 % des cas), plus rarement sur une hépatopathie chronique non cirrhotique, exceptionnellement sur un foie sain. Dans les cas de CHC développés sur cirrhose, le pronostic et la démarche thérapeutique sont ainsi conditionnés à la fois par le stade du cancer et par la fonction hépatique.
Diagnostic du Carcinome Hépatocellulaire
Le diagnostic d’un carcinome hépatocellulaire est le plus souvent évoqué après la découverte d’une lésion hépatique à l’échographie plus rarement devant des symptômes secondaires à une tumeur évoluée. Parfois c’est devant un patient qui présente une première décompensation d’une cirrhose (ascite et/ou hémorragie digestive) qu’est découvert un ou plusieurs nodules du foie.
La preuve histologique, c’est à dire l’analyse du tissu après une biopsie, doit rester obligatoire afin de confirmer le diagnostic. La biopsie reste donc la référence pour le diagnostic de carcinome hépatocellulaire, sauf en cas de contre-indication à toutes biopsies.
Examen clinique
L’examen clinique va rechercher, si le diagnostic de cirrhose n’était pas connue auparavant, des éléments permettant de confirmer ce terrain. La cirrhose en effet, peut-être asymptomatique et il faut alors systématiquement rechercher des signes d’insuffisance hépato-cellulaire et d’hypertension portale (voir le chapitre correspondant ).
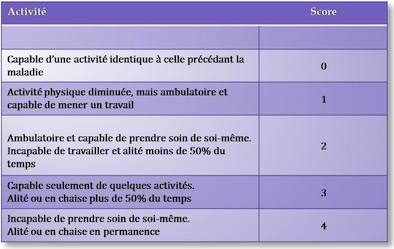
Dans ce contexte particulier et en prévision d’un geste thérapeutique que nous détaillerons plus loin, l’état général et l’activité doivent être évaluées par l’utilisation d’une échelle d’autonomie (ou « Performance Status » en anglais) et en particulier l’échelle de l’Organisation Mondiale de la Santé (OMS) qui va de 0 à 4, zéro étant la valeur « normale » (Figure n°1).
Examens biologiques
Il faut demander le Taux de Prothrombine (TP), la numération plaquettaire, l’albuminémie, la bilirubinémie, les taux des ALAT et des ASAT. Ces éléments permettront ainsi de déterminer le score de Child-Pugh et de MELD (Model for end-stage liver disease).
Il faudra bien entendu rechercher les signes d’hypertension portale par endoscopie.
Hormis ces différents examens biologiques qui permettent de réaliser le bilan de la cirrhose du foie (Voir bilan d’une cirrhose compensée), le dosage du taux alpha-fœtoprotéine (AFP) est nécessaire.
En effet, son taux peut permettre d’aider au diagnostic mais attention, son taux peut-être parfois normal alors qu’il existe un véritable carcinome hépatocellulaire et une élévation de l’alpha-fœtoprotéine, même supérieure à 400 ng/ml n’est pas suffisante pour poser le diagnostic de CHC si elle est isolée.
En revanche l’alpha-fœtoprotéine semble intervenir comme un très bon marqueur pronostique en cas de petit carcinome hépatocellulaire et peut dans certains cas être un facteur de mauvais pronostic pour des taux supérieur à 1000 ng/ml.
Examens radiologiques
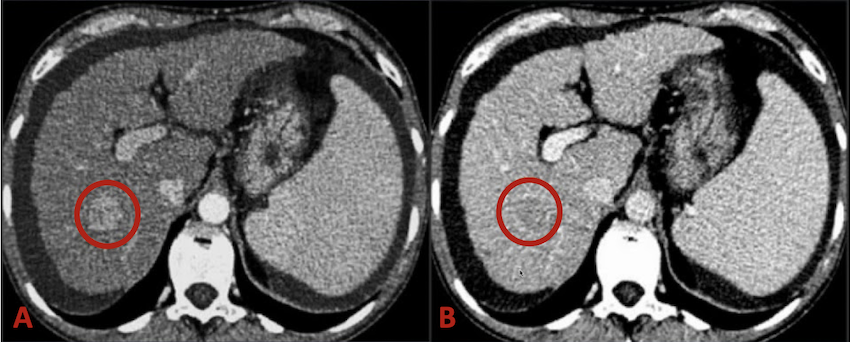
–> Le scanner hélicoïdal permet de mettre en évidence des signes très évocateurs de CHC qui sont en rapport avec sa vascularisation. En effet le Carcinome Hépatocellulaire est une tumeur qui est hypervasculaire qui va se remplir et se vider très rapidement de sang artériel.
Le nodule va apparaître hypervascularisé au temps artériel précoce (wash-in) et va très rapidement se vider (wash-out) au temps portal réalisant alors une hypodensité par rapport au foie non tumoral.
–> L’Imagerie par Résonance Magnétique (IRM) peut-être utilisée pour améliorer le diagnostic car elle permet de mieux différencier un nodule de régénération d’un nodule cancéreux.
–> L’échographie de contraste plus récente peut aussi permettre de caractériser la vascularisation du nodule avec semble-t-il une meilleure sensibilité pour dépister l’hypervascularisation que le scanner. Mais il apparaît que d’autres cancers (cholangiocarcinomes) peuvent avoir la même cinétique à l’échographie : c’est pour cette raison qu’elle n’est pas recommandée pour le diagnostic du CHC
Biopsie hépatique
Comme nous l’avons vu précédemment, la biopsie du nodule suspect d’être un carcinome hépatocellulaire doit-être réalisée afin d’avoir la certitude du diagnostic après une analyse histologique.
Cette analyse histologique devra être obtenue par une ponction dirigée sous échographie ou sous scanner. Lors de ce geste, une biopsie à coté de la tumeur, sera aussi réalisée afin d’avoir l’analyse du foie non tumoral et ainsi permet d’avoir le diagnostic certain d’une cirrhose.
Chez les patients ne pouvant pas bénéficier d’une biopsie compte-tenu de contre-indications, on peut utiliser des critères non invasifs validés.
Le diagnostic de Carcinome Hépatocellulaire peut être retenu pour les nodules de diamètre supérieur à 1 cm si lors de l’exploration radiologique, décrite ci-dessus, l’aspect est typique de CHC (nodule hypervascularisé à la phase artérielle avec wash-out à la phase portale ou à la phase tardive).
Les nodules de diamètre inférieur ou égale à 1 cm doivent être surveillés par échographie (et/ou TDM ou IRM) tous les 3 mois. S’il n’y a pas d’augmentation du diamètre avec un recul de 2 ans, on peut revenir à surveillance échographique tous les 6 mois.
Certains éléments peuvent orienter vers le diagnostic de Carcinome Hépatocellulaire :
- Age > 55 ans
- Sexe masculin
- Cirrhose évoluée et compliquée
- Un nodule ayant une taille qui augmente lors de la surveillance
- Une augmentation associée de l’ alpha-fœtoprotéine
- La présence d’une obstruction de la veine porte évoquant une obstruction vasculaire tumorale (hypervascularisation et élargissement de la veine),
Évaluation de l’extension tumorale, du terrain et de l’état général
De nombreux examens complémentaires seront réalisés afin de pouvoir poser l’indication thérapeutique notamment si une transplantation est envisagée. En effet, il peut apparaître, lors du bilan, d’autres pathologies, surtout si le patient présente une cirrhose alcoolique et un tabagisme ancien associé.
Le bilan comporte en outre un scanner thoracique ou scanner thoraco-abdominal afin de vérifier le poumon, la présence de ganglions (adénopathies) voir de métastases ainsi que le retentissement sur les voies biliaires. On recherchera une insuffisance cardiaque ou respiratoire, un cancer broncho-pulmonaires, ORL ou de l’œsophage.
Le scanner permettra aussi de réaliser le calcul du volume hépatique si une résection de la tumeur est envisagée afin d’évaluer le volume de foie restant.
Les différents traitements
La transplantation est considérée comme le traitement «idéal» car traitant la tumeur et sa cause mais elle est parfois pas possible. La résection du ou des nodules doit-être discutée chez les patients ayant une fonction hépatique normale et selon le degré d’hypertension portale. La destruction percutanée par radiofréquence ou par alcoolisation percutanée peut-être proposée. De nombreuses autres possibilités thérapeutiques existent que nous ne détailleront pas ici mais que votre médecin pourra vous expliquer selon votre bilan.
Une synthèse remarquable sur le sujet et qui est remise à jour régulièrement est située sur le site de la Société Nationale Française de Gastro-entérologie –> Thésaurus National de Cancérologie Digestive – TNCD
Références :
- Afdhal NH, Nunes D. Evaluation of liver fibrosis: a concise review. Am J Gastroenterol 2004;99(6):1160-74.
- Angulo P. Nonalcoholic fatty liver disease. N Engl J Med 2002;346:1221-31.
- Angulo P, Hui JM, Marchesini G, Bugianesi E, George J, Farrell GC, et al. The NAFLD fibrosis score: a noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology 2007;45(4):846-54.
- Bacon B.R, Adams P.C, Kowdley K.V, Powell L.W, Tavill A.S. Diagnosis and Management of Hemochromatosis: 2011 Practice Guideline by the American Association for the Study of Liver Diseases. Hepatology. 2011;54(1):328-43.
- Blanc JF, Bioulac-Sage P, Balabaud C, Desmoulière A. Investigation of liver fibrosis in clinical practice. Hepatol Res 2005;32(1):1-8.
- Blanc JF, Debaillon-Vesque A, Roth G, Barbare JC, Baumann AS, Boige V, Boudjema K, Bouattour M, Crehange G, Dauvois B, Decaens T, Dewaele F, Farges O, Guiu B, Hollebecque A, Merle P, Selves J, Aparicio T, Ruiz I, Bouché O; Thésaurus National de Cancérologie Digestive (TNCD); (SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO, AFEF, SIAD, SFR/FRI). Clin Res Hepatol Gastroenterol 2021 Mar;45(2):101590.
- Borroni G, Ceriani R, Cazzaniga M, Tommasini M, Roncalli M, Maltempo C, et al. Comparison of simple tests for the non-invasive diagnosis of clinicallly silent cirrhosis in chronic hepatitis C. Aliment Pharmacol Ther 2006;24(6):797-804.
- Cadranel JF. Practices of liver biopsy in France: results of a prospective nationwide survey. For the Group of Epidemiology of the French Association for the Study of the Liver (AFEF). Hepatology 2000;32:477-81.
- EASL clinical practice guidelines for the management of patients with decompensated cirrhosis. J Hepatol 2018;69:406-60.
- Este C, et al. Modeling NAFLD disease burden in China, France, Germany, Italy, Japan, Spain, United Kingdom, and United States for the period 2016–2030. J Hepatol 2018;69:896-904.
- Ghany M,Strader D.B, Thomas D.L, Seeff L.B. Diagnosis, Management, and Treatment of Hepatitis C Hepatology 2009:49(4):1335-1374.
- Lavanchy D. Hepatitis B virus epidemiology, disease burden, treatment, and current and emerging prevention and control measures. J Viral Hepat 2004;11(2):97-107.
- Lindor KD, Gershwin ME, Poupon R, Kaplan M, Bergasa NV, Heathcote EJ; American Association for Study of Liver Diseases.Primary biliary cirrhosis. Hepatology. 2009;50(1):291-308.
- Lok ASF, McMahon BJ. Chronic hepatitis B. Hepatology 2007;45:507- 539.
Mandayam S, Jamal MM, Morgan TR. Epidemiology of alcoholic liver disease. Semin Liver Dis 2004;24:217-232. - Manns M.P, Czaja A.J, Gorham J.D. Diagnosis and Management of Autoimmune Hepatitis. Hepatology 2010;51(6):1-31.
- Regev A, Berho M, Jeffers LJ, Milikowski C, Molina EG, Pyrsopoulos NT, et al. Sampling error and intraobserver variation in liver biopsy in patients with chronic HCV infection. Am J Gastroenterol 2002;97(10):2614-8.
- Roberts E.A, Schilsky M.L. Diagnosis and Treatment of Wilson Disease: An Update. Hepatology 2008;47(6):2089-111.
- Teli MR, Day CP, Burt AD, Bennett MK, James OF. Determinants of progression to cirrhosis or fibrosis in pure alcoholic fatty liver. Lancet 1995;346:987-990.
