Les complications d’un ulcère de l’estomac sont l’hémorragie, la perforation, la sténose et la transformation cancéreuse. Pour cette dernière complication seul l’ulcère gastrique peut devenir cancéreux.
L’hémorragie digestive
Il s’agit de la complication la plus fréquente des ulcères gastro-duodénaux qui peut être parfois inaugurale et qui représente 30 à 40 % des hémorragies digestives hautes.
Des facteurs de gravités existent et sont à prendre en considération. Il s’agit de la prise d’AINS, d’antiagrégants et/ou d’anticoagulants, un antécédent d’ulcère gastro-duodénal compliqué ou non compliqué et un âge supérieur à 65 ans.
L’ulcère peut entraîner une hémorragie distillante, non extériorisée qui est alors à l’origine d’une anémie par un déficit en fer réalisant une anémie microcytaire ferriprive (Figure n°1).

(Copyright Johns Hopkins Hospital – Traductions Monhepatogastro.net)
L’hémorragie peut être aiguë sous la forme d’une hématémèse (sang rouge vomi) ou d’un méléna (sang digéré très malodorant qui apparaît dans les selles) avec des signes cliniques de choc hypovolémique c’est à dire une tension artérielle basse associée à une tachycardie et à un malaise. La mortalité est alors d’environ 10 %.
Prise en charge initiale de l’hémorragie digestive
La mise en place d’une sonde naso-gastrique n’est pas recommandée en routine mais peut être envisagée pour confirmer l’origine digestive haute de l’hémorragie, lorsqu’il existe un doute, par la présence de sang dans le liquide d’aspiration. Elle sera enlevée rapidement.
Les patients avec un taux d’hémoglobine < à 7 g/dl doivent recevoir des transfusions avec une cible d’hémoglobine comprise entre 7 et 9 g/dl, s’il n’existe pas de pathologie cardiaque. Une cible d’hémoglobine plus élevée peut être alors nécessaire > 9 ou 10 g/dl.
La pratique est de commencer l’administration d’un Inhibiteur à la Pompe à Protons (IPP) de type Oméprazole par voie intraveineuse selon le schéma classique 80 mg en bolus suivi d’une perfusion à débit constant de 8 mg/heure pour les 72 premières heures, période pendant laquelle se produisent 80 % de récidive hémorragique.
L’utilisation d’érythromycine IV, une ampoule 30 mn avant l’endoscopie, permet d’améliorer la visualisation de la cavité gastrique.
Le diagnostic endoscopique devra être réalisé par la suite en urgence, dans les 24 h, après correction du choc hémodynamique permettant de confirmer l’origine ulcéreuse de l’hémorragie et de réaliser les gestes d’hémostases endoscopiques selon les caractéristiques du saignement.
Les gestes d’hémostase peuvent être l’injection d’adrénaline qui va permettre une vasoconstriction et une stimulation de l’agrégation plaquettaire, soit une électrocoagulation par plasma argon soit la mise en place d’un clips (véritable petite pince qui va « cliper » le vaisseau qui saigne (Figure n°2 et 3).

(Copyright Johns Hopkins Hospital – Traductions Monhepatogastro.net)

Les patients ayant des lésions endoscopiques à faible risque ne justifient pas d’un geste d’hémostase endoscopique et peuvent ressortir dés la réalisation de l’endoscopie, sous réserve de l’absence de pathologies associées importantes. La prescription d’un IPP à dose conventionnelle (Oméprazole 20 mg/jour) est alors suffisante.
Tous les patients qui présentent des lésions digestives à haut risque doivent bénéficier d’un geste endoscopique d’hémostase et être surveillés de manière appropriée, soit dans un service de réanimation, soit dans une unité d’hémorragies digestives. La réalisation d’une endoscopie de contrôle par la suite, doit se discuter au cas par cas, si l’efficacité du geste d’hémostase endoscopique est douteuse ou si le patient à un risque particulièrement élevé de récidive hémorragique.
Dans certains cas l’hémorragie ne peut pas être contrôlée et/ou récidive malgré une prise en charge endoscopique. Deux possibilités peuvent être alors proposées selon l’état clinique du patient :
Une chirurgie qui va alors consister à une fermeture chirurgicale de l’ulcère soit à une ablation d’une partie de l’estomac.
Une embolisation par radiologie interventionnelle qui est une technique permettant de fermer un ou plusieurs vaisseaux sanguins qui sont responsables du saignement.
On insère dans un cathéter, qui est un petit tube flexible en plastique ou en caoutchouc, soit un « coils » (ressort métallique) soit de la colle qui va entrainer une « thrombose ». L’extrémité du cathéter se trouvant à l’intérieur ou à proximité du vaisseau responsable de l’hémorragie (Figure n°4).
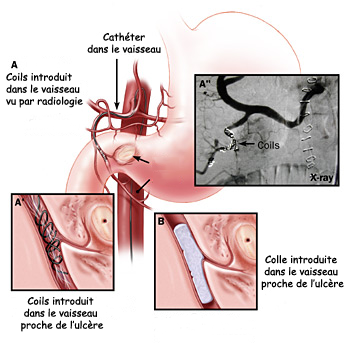
La perforation ulcéreuse
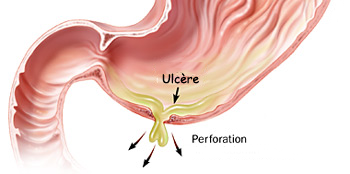
C’est une complication moins fréquente que l’hémorragie. Elle est favorisée par la prise d’AINS. Il peut s’agir d’une perforation en péritoine libre caractérisé par une douleur épigastrique intense en « coup de poignard » débutant très brutalement. L’examen clinique retrouve une contracture d’abord épigastrique puis généralisée, la disparition inconstante de la matité pré-hépatique et un cul-de-sac de Douglas douloureux au toucher rectal (Figure n°5).
Le diagnostic est confirmé par la présence d’un pneumopéritoine sur les radiographies de l’abdomen sans préparation (ASP) ou parfois vu seulement sur le scanner abdominal avec une réaction inflammatoire de la région antro-pyloro-bulbaire.
La perforation est une urgence chirurgicale qui nécessite une intervention.
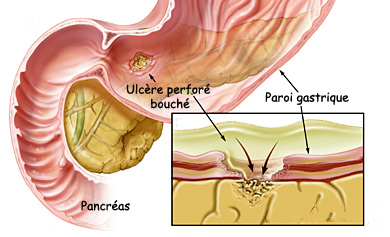
Dans certains cas, la perforation se fait au contact d’un organe de voisinage, notamment le pancréas réalisant un ulcère perforé-bouché avec comme caractéristiques une régression d’un syndrome douloureux initial, pas de pneumopéritoine ou présence d’un rétro-pneumopéritoine visible au mieux sur un scanner et une évolution possible vers la formation d’un abcès (Figure n°6).
La sténose ulcéreuse
Elle est exceptionnelle et complique les ulcères bulbaires et pré-pyloriques avec une composante fibreuse et une composante inflammatoire.
La sténose ulcéreuse est révélée par des vomissements post-prandiaux tardifs. Le diagnostic de sténose est posé par l’endoscopie éventuellement complétée par un transit baryté. Des biopsies sont nécessaires pour éliminer un cancer ou un lymphome. Le traitement sera une dilatation par un ballonnet comme nous pouvons le voir sur les figures suivantes (Figure n°7 et 8).
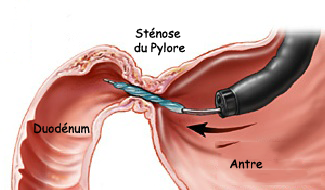

La transformation cancéreuse
Le risque de transformation cancéreuse sur les berges d’un ulcère gastrique initialement bénin est faible. La muqueuse à distance de l’ulcère gastrique peut aussi se cancériser en cas d’infection par H. pylori en raison de l’existence d’une gastrite chronique atrophiante multi-focale qui est une condition pré-cancéreuse réalisant maintenant la séquence bien connue : gastrite aiguë / atrophie / métaplasie / dysplasie / cancer invasif.
Ces risques justifient la réalisation de biopsies systématiques sur les berges ulcéreuses et à distance de l’ulcère gastrique. C’est pour cette raison qu’après un ulcère gastrique, même d’apparence bénin, il faut toujours refaire une gastroscopie à distance environ 4 à 8 semaines après pour confirmer la guérison et refaire des biopsies.
Les ulcères duodénaux ne deviennent jamais cancéreux.
Références :
- Collège des Enseignants de Gastro-entérologie – Item 290 – Ulcére gastrique et duodénal – 2004
- Dépistage de l’infection à Helicobacter pylori : pertinence et populations concernées – HAS 2010.
- Place respectives de l’endoscopie et du test respiratoire dans le diagnostic et le contrôle de l’éradication de l’Hp – HAS 2003.
- Les inhibiteurs de la pompe à protons chez l’adulte. Bon usage du médicament – HAS 2009
- Recommandations de bonne pratiques « Le bon usage des anti-sécrétoires gastriques chez l’adulte » – AFSSAPS 2007.
- Recommandations de la SFED: Techniques d’hémostase des ulcéres gastriques et duodénaux – HAS 2004.
- Management of bleeding peptic ulcer in France : a national inquiry. Lesur G, Bour B, Aegerter P – Association Nationale des Hépatogastroentérologues des Hôpitaux Généraux. Gastroenterol Clin Biol. 2005;29(2):140-4.
- Bourienne A, Pagenault M, Heresbach D, et al. Étude prospective multicentrique des facteurs pronostiques des hémorragies ulcéreuses gastroduodénales. Gastroenterol Clin Biol 2000;24:193-200.
- Lesur G, Artru P, Mitry E. Hémorragies digestives ulcéreuses : histoire naturelle et place de l’hémostase endoscopique. Gastroenterol Clin Biol 2000;24:656-66.
- Barkun AN, Bardou M, Kuipers EJ, et al. International consensus recom- mendations on the management of patients with nonvariceal upper gastrointestinal bleeding. Ann Intern Med. Jan 19 2010;152(2):101-113.
- Barkun A, Bardou M, Marshall JK. Consensus recommendations for managing patients with nonvariceal upper gastrointestinal bleeding. Ann Intern Med. Nov 18 2003; 139(10):843-857.
