L’hémorragie digestives peut-être secondaire à une rupture de varices, œsophagiennes ou gastriques, mais aussi à un saignement d’ulcères. Nous ne verrons dans cette partie que les hémorragies liées à une rupture de varices. Les hémorragies secondaires à un ulcère sont traités dans un chapitre spécifique.
L’hémorragie digestive par rupture de varices œsophagiennes (VO), peut-être la première manifestation d’une cirrhose jusqu’alors asymptomatique et s’associer d’emblée aux autres complications de la maladie qui sont l’encéphalopathie hépatique, la décompensation œdèmato-ascitique et/ou l’encéphalopathie hépatique.

L’hémorragie digestive peut se manifester de différentes façons :
– Par une Hématémèse : qui correspond à un vomissement de sang qui est toujours d’origine haute.
– Par un Méléna : qui correspond à extériorisation par l’anus de sang digéré, noir, et malodorant (aspect de goudron). Le sang étant descendu le long de l’intestin et est digéré.
– Par une Rectorragie : qui correspond à émission par l’anus de sang rouge non mélangé aux selles. Dans ce cas le patient présente le plus souvent un état de choc car l’hémorragie a été si importante que le sang est descendu dans l’intestin sans avoir eu le temps d’être digéré est transformé en méléna.
Prise en charge de l’hémorragie
Il faut rechercher dans un premier temps les critères de gravité
Le retentissement hémodynamique est le critère principal de gravité. L’examen clinique doit rechercher une pâleur, une hypotension voire un état de choc, avec des signes périphériques, associant :
- marbrures,
- sueurs,
- troubles de conscience,
- augmentation du temps de recoloration cutanée,
- oligurie.
Attention aux pièges :
- En l’absence d’extériorisation du saignement, on doit rechercher la présence de méléna au toucher rectal.
- L’existence d’une tachycardie peut être masquée par la prise de bêtabloquants.
- L’hématocrite mesuré trop précocement, lors de la prise en charge au domicile par exemple, peut sous-estimer la gravité de l’hémorragie.
Examens biologiques à demander
- Numération sanguine, Ionogramme et créatinine
- hémoglobine au doigt mais chiffre approximatif d’hémoglobinémie instantané.
- Groupe – Rhésus – RAI
- Hémostase : TP, TCA, Plaquettes.
Les malades cirrhotiques qui ont une hémorragie digestive haute doivent être transférés dans une unité de soins intensifs ou de réanimation.
- En cas d’hypotension sévère ou de choc, la première étape de la prise en charge consiste à poser deux voies veineuses périphériques de bon calibre afin d’effectuer un remplissage vasculaire.
- Une endoscopie doit être pratiquée en urgence, le plus rapidement possible, et de toute façon dans les 12 heures, chez un malade à jeun, conscient, coopérant et stable sur le plan hémodynamique.
- Une transfusion globulaire est justifiée en cas de mauvaise tolérance de l’anémie ou si le taux d’hémoglobine est inférieur à 7 g/dL. L’objectif de la transfusion est d’obtenir un taux d’hémoglobine à 7-8 g/dL.
- Attention : la mise en place d’une sonde nasogastrique n’est pas recommandée.
Une perfusion d’érythromycine avant la gastroscopie permet d’accélérer rapidement la vidange de l’estomac et d’améliorer les conditions de l’endoscopie. Attention l’érythromycine est contre-indiquée en cas de QT long à l’ECG.
Traitements spécifiques
Traitement vasoactif destiné à réduire la pression portale doit être institué en urgence. Il repose sur l’administration intraveineuse soit de somatostatine ou d’analogues de la somatostatine (octréotide) soit de dérivés de la vasopressine (terlipressine). Ce traitement doit être administré pendant 2 à 5 jours. Au-delà, un relais doit être pris par des bêtabloquants au long cours.
Une Antibiothérapie est habituellement recommandée systématiquement car les épisodes d’hémorragie digestive par rupture de varices œsophagiennes chez les patients cirrhotiques se compliquent fréquemment d’une infection bactérienne. Ainsi une antibioprophylaxie systématique est justifiée pendant 7 jours par quinolone (norfloxacine), ou amoxicilline-acide clavulanique ou céphalosporine de 3e génération (cefotaxime) pendant 7 jours.
L’endoscopie digestive haute est donc l’examen à réaliser obligatoirement dans les 12 heures qui suivent l’épisode d’hémorragie digestive.
Une préparation reposant sur l’administration préalable d’érythromycine, 30 minutes avant l’endoscopie digestive haute, par voie intraveineuse est nécessaire. Cette molécule stimule la motricité gastrique et permet ainsi de vidanger l’estomac.
L’endoscopie permet d’une part de confirmer le diagnostic et de réaliser un geste thérapeutique qui peut-être la réalisation d’une ligature d’une varice œsophagienne ou bien l‘injection d’un produit sclérosant comme cela est réalisée pour un ulcère hémorragique. La réalisation d’une ligature est préférable en première intention sur une varice œsophagienne hémorragique car elle permet l’arrêt d’une hémorragie active avec de meilleurs résultats (Figure n°1).
Il est à noter que l’origine d’une hémorragie par rupture de varice œsophagienne n’est retrouvée que dans 40 à 70 % des cas. Une hémorragie secondaire à un ulcère n’est donc pas rare.

En cas d’échec, on peut avoir recours à la mise en place d’une sonde de tamponnement œsophagienne par sonde de Blackemore (Figure n°2). Elle permet par pression d’effectuer un tamponnement de la zone hémorragique non contrôlable initialement par les gestes précédemment décrit (ligature et sclérose) et reste donc un geste de sauvetage lorsque l’hémorragie digestive reste active et abondante.
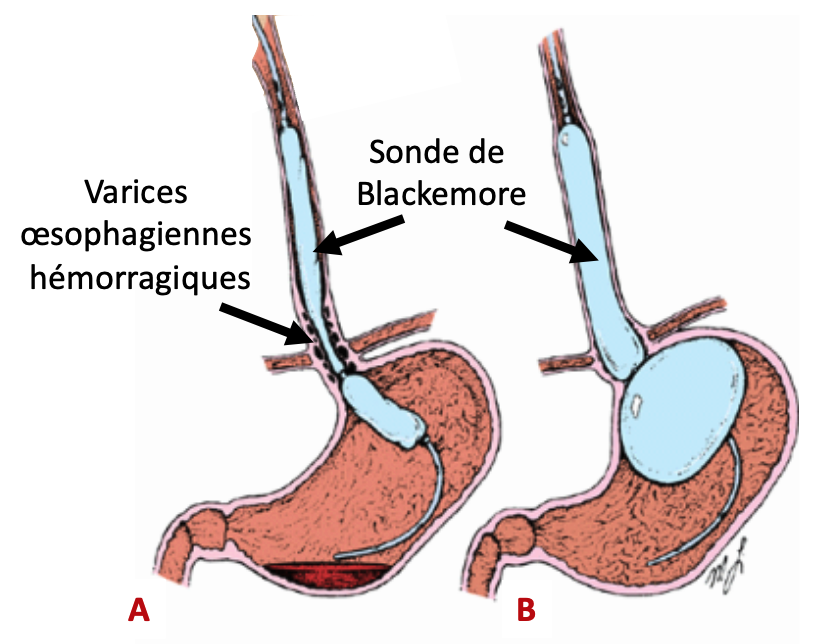
Une autre solution peut-être proposée qui est la mise en place en urgence d’une prothèse, par voie transjugulaire, qui va réaliser un shunt porto-cave intrahépatique que l’on appelle un TIPS pour « transjugular intrahepatic portosystemic shunt ». Sa mise en place est une option thérapeutique indiquée en cas d’hémorragie de varices œsophagiennes aiguë, lorsque les traitements médicamenteux et endoscopiques se sont avérés inefficaces.
L’objectif est de baisser la pression dans le système porte car le shunt intra-hépatique qui va être réalisé entre une veine hépatique et une branche de la veine porte va permettre de diminuer la pression portale (Figure n°3).

Prévention des hémorragies digestives
La prévention primaire des hémorragies digestives sur hypertension portale repose sur les endoscopies de dépistage et le traitement des varices à risque. Une endoscopie digestive haute doit systématiquement être réalisée lors de la prise en charge initiale d’une cirrhose compensée ou décompensée. Ainsi la présence de varice œsophagienne devra faire débuter des séance itératives de ligatures des varices toutes les 2 à 3 semaines.
Quatre éléments devront être recherchés systématiquement lors de l’exploration de l’estomac chez un patient en dehors d’une hémorragie digestive.
- La description des varices œsophagiennes
- Nombre de cordons.
- Leur étendue en hauteur en cm par rapport aux arcades dentaires
- Classification en 3 grades (Figure n°4).

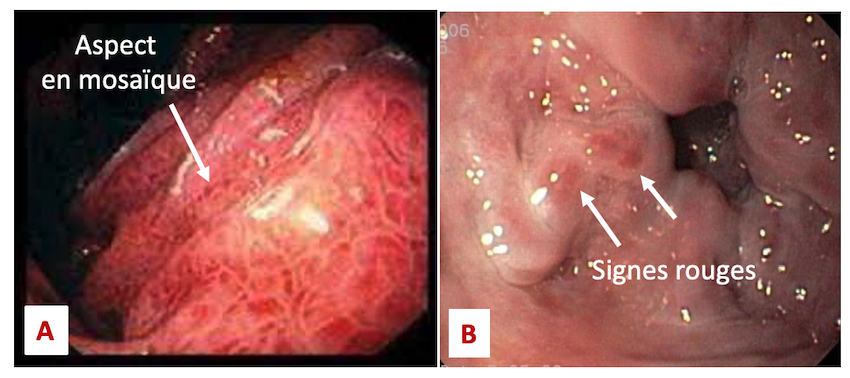
- La présences de signes rouges
- La présence d’une Gastropathie d’hypertension portale (Figure n°5).
- La présence de varice cardio-tubérositaires observées en rétrovision
La prévention secondaire correspond à la préventions des récidives chez les malades qui ont déjà eu une hémorragie digestive sur rupture de varices œsophagiennes. Dans ce cas, les bêtabloquants doivent être introduits pour prévenir les récidives chez tous les malades, en l’absence de contre-indication. Ils sont associés aussi aux ligatures de varices œsophagiennes itératives toutes les 2 à 3 semaines.
Références :
- Afdhal NH, Nunes D. Evaluation of liver fibrosis: a concise review. Am J Gastroenterol 2004;99(6):1160-74.
- Angulo P. Nonalcoholic fatty liver disease. N Engl J Med 2002;346:1221-31.
- Angulo P, Hui JM, Marchesini G, Bugianesi E, George J, Farrell GC, et al. The NAFLD fibrosis score: a noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology 2007;45(4):846-54.
- Bacon B.R, Adams P.C, Kowdley K.V, Powell L.W, Tavill A.S. Diagnosis and Management of Hemochromatosis: 2011 Practice Guideline by the American Association for the Study of Liver Diseases. Hepatology. 2011 ;54(1):328-43.
- Blanc JF, Bioulac-Sage P, Balabaud C, Desmoulière A. Investigation of liver fibrosis in clinical practice. Hepatol Res 2005;32(1):1-8.
- Borroni G, Ceriani R, Cazzaniga M, Tommasini M, Roncalli M, Maltempo C, et al. Comparison of simple tests for the non-invasive diagnosis of clinicallly silent cirrhosis in chronic hepatitis C. Aliment Pharmacol Ther 2006;24(6):797-804.
- Cadranel JF. Practices of liver biopsy in France: results of a prospective nationwide survey. For the Group of Epidemiology of the French Association for the Study of the Liver (AFEF). Hepatology 2000;32:477-81.
- EASL clinical practice guidelines for the management of patients with decompensated cirrhosis. J Hepatol 2018; 69:406-60.
- Este C, et al. Modeling NAFLD disease burden in China, France, Germany, Italy, Japan, Spain, United Kingdom, and United States for the period 2016–2030. J Hepatol 2018; 69:896-904.
- Ghany M,Strader D.B, Thomas D.L, Seeff L.B. Diagnosis, Management, and Treatment of Hepatitis C Hepatology 2009:49 (4):1335-1374.
- Lavanchy D. Hepatitis B virus epidemiology, disease burden, treatment, and current and emerging prevention and control measures. J Viral Hepat 2004;11(2):97-107.
- Lindor KD, Gershwin ME, Poupon R, Kaplan M, Bergasa NV, Heathcote EJ; American Association for Study of Liver Diseases.Primary biliary cirrhosis. Hepatology. 2009 Jul;50(1):291-308.
- Lok ASF, McMahon BJ. Chronic hepatitis B. Hepatology 2007;45:507- 539.
Mandayam S, Jamal MM, Morgan TR. Epidemiology of alcoholic liver disease. Semin Liver Dis 2004;24:217-232. - Manns M.P, Czaja A.J, Gorham J.D. Diagnosis and Management of Autoimmune Hepatitis. Hepatology. 2010 ;51(6):1-31.
- Regev A, Berho M, Jeffers LJ, Milikowski C, Molina EG, Pyrsopoulos NT, et al. Sampling error and intraobserver variation in liver biopsy in patients with chronic HCV infection. Am J Gastroenterol 2002;97(10):2614-8.
- Roberts E.A, Schilsky M.L. Diagnosis and Treatment of Wilson Disease: An Update. Hepatology. 2008 ;47(6) :2089-111.
- Teli MR, Day CP, Burt AD, Bennett MK, James OF. Determinants of progression to cirrhosis or fibrosis in pure alcoholic fatty liver. Lancet 1995;346:987-990.
